5. Compuestos nitrogenados: aminas, amidas y nitrilos
Objetivos
- Reconocer los diferentes compuestos orgánicos nitrogenados no proteicos.
- Aplicar la metodología de la nomenclatura IUPAC de compuestos orgánicos nitrogenados.
- Comprender la aplicación industrial de aminas, amidas y nitrilos.
5.1. Aminas
Las aminas resultan de la sustitución de uno, dos o tres átomos de hidrógeno del amoníaco por radicales alquílicos o aromáticos. Dependiendo del número de hidrógenos que se sustituyan, se obtienen aminas primarias, secundarias y terciarias. Se nombran indicando los radicales por orden alfabético y la terminación -amina.
|
Aminas primarias |
R-NH |
un enlace C-N, dos enlaces N-H. |
|---|---|---|
|
Aminas secundarias |
R-NH-R' |
dos enlaces C-N, un enlace N-H |
|
Aminas Terciarias |
R-N-R'|R'' |
tres enlaces C-N, ningún enlace N-H |
Clasifique las siguientes aminas en primarias, secundarias o terciarias.
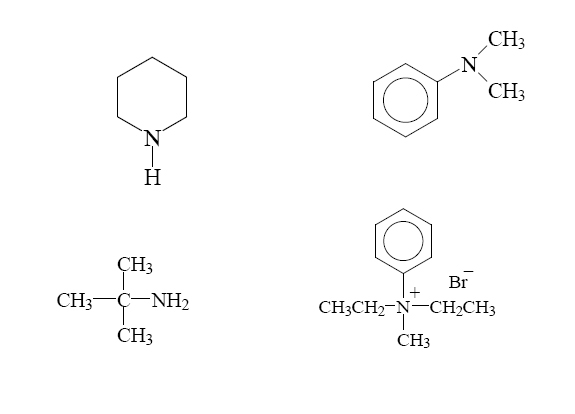
Las aminas son compuestos nitrogenados con estructura piramidal, similar al amoniaco (NH3). Forman parte de las células vivas y algunas son biológicamente importantes. Están presentes en ácidos nucleicos, vitaminas, coenzimas y hormonas, como la adrenalina. Son parte de los alcaloides, compuestos complejos que se encuentran en las plantas, como la morfina y la nicotina. Se emplean en las industrias química, farmacéutica, de caucho, de curtidos y cueros, plásticos, colorantes, tejidos, cosméticos y metales.
La amina con un átomo de carbono es gaseosa, las que tienen de dos a once átomos de carbono son líquidas y las demás sólidas. Las primeras son muy solubles en agua, luego la solubilidad va disminuyendo con la cantidad de átomos de carbono. Los primeros miembros de esta serie poseen un olor similar al amoníaco, pero a medida que aumentan los carbonos el olor se asemeja al del pescado. A diferencia del amoníaco arden en presencia de oxígeno por tener átomos de carbono.
Las aminas son bases y forman soluciones fuertemente alcalinas, por lo que pueden resultar dañinas si salpican los ojos o si contaminan la piel. Las aromáticas (que contienen uno o más anillos de benceno) son muy tóxicas y se absorben a través de la piel. Sin embargo, las aminas alifáticas inferiores carecen de propiedades tóxicas específicas y forman parte de los tejidos corporales. Estos compuestos se encuentran en un gran número de alimentos, como el pescado, al que dan su olor característico. Una preocupación actual es la posibilidad de que algunas aminas alifáticas puedan reaccionar con nitratos o nitritos in vivo para formar compuestos nitrosos, muchos de los cuales son cancerígenos potentes en animales.
Formación de nitrosaminas
Las nitrosaminas son aminas que contienen un grupo funcional nitroso (–N–N=O), que se forman cuando un nitrógeno (N) y un oxígeno (O) de un compuesto “nitrosante” se unen al nitrógeno del grupo amino (N) de un compuesto amínico. Esta reacción sucede, por ejemplo, cuando las sales de nitrato y nitrito utilizadas en los baños de sal para la fabricación de caucho sirven de agentes nitrosantes y se combinan con aminas en el caucho, formando nitrosaminas. Estas también pueden formarse in vivo durante el metabolismo de alimentos que contienen nitratos o nitritos.
La formación de estos compuestos es preocupante, ya que existen pruebas de que podrían causar cáncer en el ser humano. Ensayos experimentales han demostrado que las nitrosaminas son potentes cancerígenos en animales.
La formación de nitrosaminas en operaciones como las de la industria del caucho puede evitarse reformulando los compuestos de caucho o utilizando métodos alternativos, como aire caliente con perlas de vidrio o curado con microondas. Sin embargo, realizar estas modificaciones requiere de investigación para lograr un producto final con las mismas propiedades que el producto de caucho obtenido con métodos tradicionales. Otra posibilidad para reducir las exposiciones es la ventilación por extracción localizada (VEL) y controles técnicos adecuados para garantizar que las exposiciones de los trabajadores se mantengan reducidas.
Fuente: Enciclopedia de salud y seguridad en el trabajo (1998).
5.1.1. Nomenclatura
Se forman con los nombres de los grupos alquilo enlazados al nitrógeno, seguidos del sufijo –amina. Se utilizan los prefijos di-, tri- y tetra- para indicar que hay dos tres o cuatro sustituyentes idénticos.
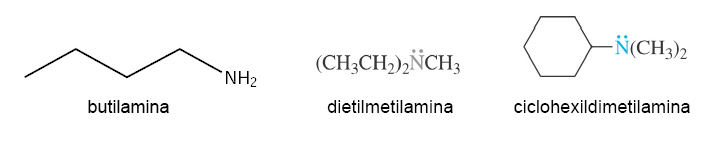
En una molécula con un grupo funcional de mayor prioridad, la amina se nombra como sustituyente.
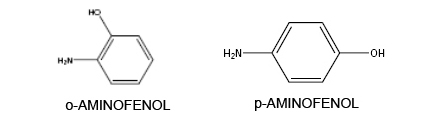
Las aminas arómáticas normalmente son conocidas por sus nombres triviales; por ejemplo, la fenilamina, denominada comúnmente como anilina.

Aminas heterocíclicas
Al heteroátomo se le asigna el número 1.

La cadena principal es la que contiene mayor número de átomos de carbono, se sustituye la terminación -o del alcano por -amina. Los sustituyentes del nitrógeno tienen un prefijo N-.
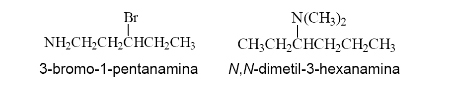
5.1.2. Aminas aromáticas
Las aminas aromáticas constituyen un amplio grupo de compuestos químicos de gran interés industrial y comercial. Derivan de los hidrocarburos aromáticos, como benceno, tolueno y naftaleno. La anilina es la amina aromática más simple y utilizada comercialmente consta de un grupo -NH2 unido a un anillo de benceno.
Las aminas aromáticas se utilizan principalmente como compuestos intermedios en la fabricación de tintes y pigmentos. Los compuestos azoicos son algunos de los colorantes más comunes de diversos tipos, como colorantes directos, ácidos, básicos, de naftol, mordentes ácidos, dispersos, etc., y se utilizan ampliamente en tejidos, telas, artículos de piel, productos de papel, plásticos y muchos otros artículos.
Con muchos de estos compuestos se deben tomar las precauciones necesarias para manipular sustancias carcinógenas. Las aminas aromáticas naftilaminas y aminoantracenos han mostrado problemas de carcinogenicidad.
Anilinas
Las anilinas se utilizan principalmente como productos intermedios en la fabricación de colorantes y pigmentos. Algunas de ellas son también sustancias intermedias en la fabricación de productos farmacéuticos, herbicidas, insecticidas y sustancias químicas para el procesado del caucho.
La propia anilina se utiliza ampliamente en la fabricación de colorantes sintéticos, tintas para imprenta y tintes textiles, así como en la fabricación de resina, barnices, perfumes, colorantes para zapatos, productos químicos para fotografía, explosivos, herbicidas y fungicidas. Se emplea en la fabricación del caucho y como agente de vulcanización, antioxidante y agente antiozono. Otra aplicación importante de la anilina es en la fabricación del p,p’-metilen-bisfenildiisocianato (MDI), que se utiliza para preparar resinas de poliuretano y fibras spandex y para adherir caucho al rayón y al nylon.
Estructura química de la anilina
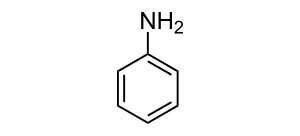
La fenilamina, comúnmente conocida como anilina (\(C_6H_5NH_2\)), es un compuesto líquido, incoloro, soluble en disolventes orgánicos y ligeramente en agua. El término anilina proviene del nombre específico añil, derivado de la palabra sánscrita nila (índigo).
Fue descubierta en 1856, cuando el químico británico William Henry Perkin, al ensayar la oxidación de la anilina, obtuvo un precipitado violeta que servía como tinte estable y resistente a la luz. El color obtenido, el violeta, se convertiría en el primer tinte sintético y había sido el pigmento más difícil de obtener de forma natural, siendo desde tiempos fenicios un gran negocio.
Con solo 18 años, Perkin patentó la idea y puso en marcha una fábrica para su producción a gran escala en Greenford Green, Middlesex. Al principio se llamó anilina tinte púrpura, pero, después de su éxito en Francia, fue rebautizado malva (o mauveine). La empresa fue un gran éxito y poco tiempo después, otros tintes sintéticos, elaborados a partir de la fenilamina y de derivados del alquitrán de hulla, estaban compitiendo en el mercado con los tintes naturales.
El nuevo invento se hizo muy popular, no solo por su costo de producción, sino por el brillo, la perdurabilidad del tono, la capacidad de lavado y la resistencia a la luz.
De esta forma, los colores malvas, azules y otros derivados de la anilina inundaron la industrial textil, de manera que los años que van de 1850 a 1860 se han denominado la «década malva».
Industrialmente, el modo más asequible de preparar la fenilamina para su uso comercial consiste en reducir el nitrobenceno mediante hierro y ácido clorhídrico. También se puede preparar comercialmente a través de la acción del amoníaco a alta presión sobre el clorobenceno en presencia de un catalizador. En ambos casos, la materia prima se obtiene a partir de benceno. Actualmente, el principal uso de la fenilamina es la producción de una clase importante de plásticos llamados poliuretanos. También tiene otras importantes aplicaciones como la elaboración de tintes, medicinas (la sulfanilamida, por ejemplo), explosivos y muchos otros productos sintéticos.
Fuente: Fagin (2013).
Riesgos para la salud
El empleo industrial de algunas aminas aromáticas puede implicar un riesgo grave para la salud de los trabajadores. Esto se debe a la facilidad con que pueden ser absorbidas por vía respiratoria o percutánea, ya que en su mayoría las aminas aromáticas son liposolubles. Por otro lado, la absorción por vía digestiva constituye un peligro potencial si no se cuenta con instalaciones sanitarias y comedores adecuados. La contaminación de los alimentos y el fumar con las manos sucias son dos ejemplos de posibles vías de ingestión. Por ello, la prevención de la intoxicación por anilinas exige un conocimiento exhaustivo de las normas de higiene personal e industrial
Las aminas aromáticas tienen efectos patológicos diversos y diferentes para cada especie, sin embargo, comparten algunos efectos importantes, como el cáncer de las vías urinarias, riesgo de intoxicación aguda y sensibilización cutánea y respiratoria.
Los potentes efectos cancerígenos de las aminas aromáticas se descubrieron en el ámbito laboral, por primera vez, en una fábrica de colorantes, por lo que se denominó en un principio “cáncer por tintes”. Finalmente, se estableció que estas patologías se deben a las materias primas utilizadas para elaborar los colorantes, entre las que se encuentra la anilina, por cuya razón se denominaron en forma general como “cánceres por anilina”. Fue más tarde cuando se identificó que la verdadera causa de estos cánceres se debe a la b-naftilamina y a la bencidina.
Unos 180.000 trabajadores, expuestos a los efectos cancerígenos de las aminas aromáticas
Por Milagros Pérez Oliva
Hace tres años, el equipo médico del hospital de Sant Jaume y Santa Magdalena de Mataró observó, a la luz de los datos obtenidos en los registros de tumores y de hospitalización, que el número de casos de cáncer de vejiga atendidos en el centro era totalmente anormal. El porcentaje alcanzaba el 12% de todos los casos de cáncer, cuando el porcentaje medio en España era del 5,8%. Solo había dos explicaciones: que hubiese alguna razón especial para que los tumores más frecuentes no llegasen al hospital, falseando de este modo las estadísticas, o que realmente existiese en la comarca algún factor que provocase un exceso de morbilidad y mortalidad por cáncer de vejiga. Descartada la primera hipótesis, el hospital encargó al doctor Carlos A. González, jefe del Servicio de Epidemiología y Estadística, que iniciase una investigación a partir de la segunda hipótesis. De hecho, era presumible que hubiese un exceso de mortalidad, pues está perfectamente demostrada la relación que existe entre el cáncer de vejiga y la manipulación de ciertos productos utilizados en la industria del tinte y los colorantes.
Concentración industrial
Mataró y su comarca presentan una elevada concentración de industria textil y, por lo tanto, de empresas subsidiarias de tinte y estampado. Las primeras investigaciones confirmaron plenamente las sospechas. Según el censo ocupacional de 1975, el 32,64% de la población activa de Mataró trabajaba en la industria textil. Por su parte, el registro de recaudación de impuestos industriales del Ayuntamiento del año 1980 tenía registradas en la ciudad 34 empresas de estampados, siete de fabricación de artículos de caucho, cinco de pinturas y tres de barnices.
Hechas estas comprobaciones, el doctor González inició su estudio analizando la mortalidad por cáncer de vejiga registrada en Mataró entre 1978 y 1980 a partir de los datos estadísticos del Registro Civil. Aun teniendo en cuenta que la mortalidad de esta localidad está subestimada, pues muchos enfermos son hospitalizados y mueren en Barcelona, la conclusión fue tajante: “Se producen en Mataró casi el doble de casos de cáncer de vejiga de los que deberían producirse si la tasa fuera similar a la del resto de España”. Exactamente, en España se producían 4,67 muertes por cada 100.000 habitantes y en Mataró se registraban 7,45.
El riesgo ocupacional
El doctor González analizó después la incidencia de los factores de sexo y edad, muy importantes en esta enfermedad. El cáncer de vejiga representa en España el 5,8% del total de casos nuevos de cáncer por año en el sexo masculino. El riesgo de contraer esta enfermedad es siete veces superior en el hombre que en la mujer, y aunque la tasa de incidencia comienza a ascender después de los 40 años, normalmente el mayor riesgo se concentra en los años de la llamada tercera edad. Una vez comprobados las anteriores datos y consultada la abundante bibliografía internacional que existe sobre la relación entre la manipulación de ciertos productos químicos y el cáncer de vejiga, el doctor González, en colaboración con los miembros del servicio de Epidemiología y Estadística, inició en marzo de 1981 un estudio pormenorizado del proceso seguido por 58 enfermos fallecidos entre el 1 de enero de 1979 y el 31 de julio de 1981, seleccionados en dos fuentes: las defunciones del Registro Civil y los ingresos en el hospital de Mataró.
El tabaco aumenta el riesgo
Se analizó primero la incidencia que podían tener en estos casos otros factores de riesgo, como el consumo de café y tabaco, cuya relación con el cáncer es reconocida también internacionalmente. Está demostrado, por ejemplo, que el riesgo de contraer cáncer de vejiga es 2 o 3 veces superior en los fumadores que en los no fumadores. Los resultados demostraron una incidencia muy nociva del hábito de fumar. El consumo de café, por el contrario, no implica, según el estudio, un incremento del riesgo de contraer el cáncer de vejiga.
Se consideraron expuestos los trabajadores de las siguientes ocupaciones: preparación y obtención de productos químicos; refino del petróleo; blanqueo, tinte y acabado de productos textiles; curtido de pieles; fabricación de productos de caucho y plásticos; fabricación y vulcanización de neumáticos; ciertos trabajos de artes gráficas y el estampado textil.
El estudio llegó a la conclusión de que “si se eliminara la exposición profesional, se podría reducir en un 12% el número de casos de cáncer de vejiga que se producen anualmente en la población general”. El índice de riesgo por factores profesionales es, según el estudio, del 5,73. Es decir, que un trabajador que ha permanecido un mínimo de un año expuesto tiene 5,73 veces más posibilidades de morir de un cáncer de vejiga que un trabajador no sometido a este riesgo. Este porcentaje aumenta hasta el 10,86 en el caso de los trabajadores expuestos que además fuman 20 o más cigarrillos diarios.
“El riesgo de los fumadores que han trabajado uno o más años en ocupaciones consideradas expuestas es 11 veces superior a los que no fuman y tienen otro tipo de ocupación”, señala el informe. La asociación del hábito de fumar y la exposición profesional a productos cancerígenos tiene, pues, un peligroso efecto multiplicador. Según el estudio, si se eliminara simultáneamente la exposición ocupacional y el hábito de fumar, podría evitarse el 40,7% de los casos de cáncer de vejiga que se dan en la población general.
Ocho mil empresas
Los resultados obtenidos en el informe del doctor Carlos A. González son muy similares a los obtenidos por estudios realizados en Inglaterra, Estados Unidos, Canadá e Italia sobre trabajadores expuestos al riesgo de los aminoderivados de los hidrocarburos aromáticos. Se calcula que el periodo de latencia, entre que se inicia la exposición del trabajador hasta que aparece el cáncer, es de unos 18 años. Los autores del informe mantuvieron contactos con empresarios de la comarca, quienes reconocieron utilizar las sustancias cancerígenas.
Según datos facilitados por la Federación Española de Industrias Químicas, en 1979 se consumían en España 1395 toneladas de productos derivados de las aminas aromáticas. Concretamente, 985 toneladas de alfa-naftilamina, todas ellas de importación; 400 toneladas de fenil beta-naftilamina, producidas especialmente en las provincias de Álava y Barcelona; y 10 toneladas de orto-tolouidina, también de importación.
El Instituto Nacional de Empleo, por su parte, afirma que en 1977 (último año del que se disponen estadísticas) se produjeron en España 67.634 toneladas de colorantes y pigmentos. El informe del doctor Carlos A. González calcula, en base a las estadísticas disponibles, con criterio restrictivo, que existen en España 8135 empresas con 179.832 trabajadores presumiblemente expuestos a la acción carcinogénica de las aminas aromáticas.
Fuente: edición impresa del domingo 15/5/1983. <https://elpais.com/diario/1983/05/16/sociedad/421884003_850215.html>
Señale el nombre correcto para los siguientes compuestos:
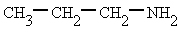
a) propilamida b) propilamina c) butilamina
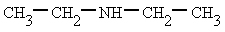
a) dietilamida b) dietildiamina c) dietilamina
-

a) N-etil-N'-propilbutanamina b) N-etil-N-propilbutanamina c) N-butil-N-etilpropanamina

a) dibencilamina b) fenildiamina c) difenilamina
Colorantes azoicos y diazoicos o tintes "azo"
Los colorantes azoicos son los más utilizados industrialmente y se caracterizan por la presencia de un grupo azo (-N=N-) en su estructura molecular que une, al menos, dos anillos aromáticos. Estos compuestos conforman el grupo químico más importante de tintes y colorantes en la idustria textil, cosmética y alimentaria. Este grupo puede dividirse en subgrupos de colorantes monoazoicos, diazoicos y triazoicos según el número de grupos azo que posea la molécula.
El proceso de obtención de los tintes "azo" se denomina diazotización, cuando una amina aromática es transformada en un componente diazonio, que reacciona con un componente de acoplamiento, como el phenol, naphtol o una amina, para formar el colorante. Por la amplia variedad de combinaciones entre componentes diazo y componentes de acoplamiento posibles, se pueden obtener un rango de variación muy amplio de los "azo-colorantes" .
5.2. Amidas
Las amidas son compuestos orgánicos que pueden derivar de ácidos o de aminas. Existen tres tipos de amidas: primarias, secundarias y terciarias, también llamadas amidas sencillas, sustituidas o disustituidas, dependiendo del grado de sustitución del átomo de nitrógeno.
Mayormente, son de naturaleza neutra en comparación con los ácidos o aminas de los que se derivan, y algunas de ellas son ligeramente resistentes a la hidrólisis. Estos compuestos son muy utilizados en la síntesis orgánica, en la industria farmacéutica y en la industria del nailon.
Las amidas poseen una gran variedad de estructuras químicas posibles provocando diversidad en sus efectos biológicos asociados a los riesgos en la salud. Algunas son completamente inocuas, por ejemplo, las amidas de los ácidos grasos simples de cadena larga, y otras están calificadas como probables cancerígenos, como la acrilamida.
La acrilamida es una sustancia química que se utiliza industrialmente en la síntesis de polímeros, colorantes, adhesivos, en el engomado del papel, en la industria textil y en el tratamiento de agua y aguas residuales. Se obtuvo por primera vez en 1893 en Alemania. Sin embargo, recién a mediados de 1950 se observó que los trabajadores expuestos a acrilamida desarrollaban alteraciones neurológicas características, asociadas principalmente con dificultades posturales y motoras.
La acrilamida además se produce en algunos alimentos. La formación de este compuesto depende de la presencia de algunos aminoácidos (principalmente la asparragina) y azúcares reductores, que reaccionan entre sí durante procesos de cocción y procesamiento a altas temperaturas de los productos alimenticios. El proceso químico que provoca la formación de acrilamida se conoce como reacción de Maillard y es responsable del oscurecimiento y cambio de sabor en el exterior de las galletas, en el pan, cerveza, café y carne asada, entre otros.
Si bien ensayos experimentales realizados in vivo e in vitro han demostrado que la exposición a acrilamida puede producir efectos cancerígenos y alteraciones en el sistema reproductivo, nervioso y genético, aún no se ha comprobado que los niveles de acrilamida producidos en los alimentos impliquen un riesgo para la salud. Sin embargo, se recomienda tomar medidas, para reducir su producción controlando la concentración de azúcares y asparragina.
Fuente: Valenzuela y Ronco (2007).
Las amidas simples derivadas de los ácidos carboxílicos alifáticos (excepto la formamida) son sólidas a temperatura ambiente, mientras que las amidas sustituidas derivadas de ácidos carboxílicos alifáticos pueden ser líquidas, con puntos de ebullición relativamente altos. Las amidas derivadas de los ácidos carboxílicos aromáticos o sulfónicos en general son sólidas. Por otro lado, las amidas sustituidas, en general, tienen propiedades disolventes muy importantes.
5.2.1. Nomenclatura
-
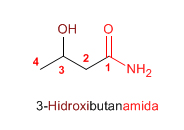
Las amidas se nombran como derivados de ácidos carboxílicos sustituyendo la terminación -oico del ácido por -amida.

-
Las amidas son grupos prioritarios frente a aminas, alcoholes, cetonas, aldehídos y nitrilos.
-
Las amidas actúan como sustituyentes cuando en la molécula hay grupos prioritarios, en este caso preceden el nombre de la cadena principal y se nombran como carbamoil.

- Dibuje la estructura de las siguientes amidas:
- Metanamida
- Butanamida
- N,N-Dimetiletanamida
- Propanodiamida
- N-Metildietanamida
Determine cuál es la nomenclatura correcta de las siguientes estructuras:
-
5.3. Nitrilos
Los nitrilos son todos aquellos compuestos orgánicos que en su molécula poseen un grupo funcional ciano (-C≡N), Pueden también considerarse derivados orgánicos del cianuro de hidrógeno en los que este último ha sido remplazado por un radical alquilo. Los nitrilos alifáticos se representan con la fórmula general RCN, mientras los nitrilos aromáticos con la fórmula ArC.
Los nitrilos pueden sufrir una gran variedad de reacciones químicas, por lo que son materia prima para un gran número de compuestos de amplio uso industrial, químico y farmacéutico.
Se utilizan en la producción de colorantes, esmaltes y pinturas, y en la fabricación de guantes de látex. Son usados también como veneno e insecticida para para combatir insectos, bacterias y hongos en la agricultura.
Los nitrilos son compuestos tóxicos y esta toxicidad depende de la estructura de cada molécula. Pueden ocasionar problemas de salud como dermatitis graves y muy dolorosas si la piel está expuesta a ellos. En casos extremos pueden ocasionar muerte por asfixia, de forma similar a la exposición al cianuro de hidrógeno. Por otro lado, se han registrado casos de personas que han sobrevivido a la exposición a concentraciones de nitrilos elevadas y no mostraron efectos fisiológicos residuales.
5.3.1. Nomenclatura
-
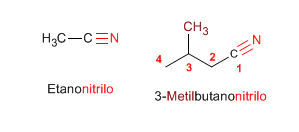
Los nitrilos se nombran añadiendo el sufijo -nitrilo al nombre del alcano con igual número de carbonos.
-
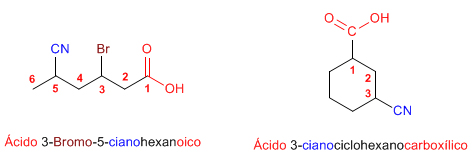
Cuando los nitrilos actúan como sustituyentes se emplea el prefijo ciano-, precediendo el nombre de la cadena principal.
-
Los nitrilos unidos a ciclos se nombran terminando el nombre del anillo en -carbonitrilo
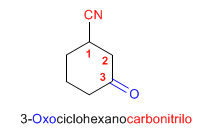
Escriba las fórmulas estructurales de los siguientes nitrilos:
- Metanonitrilo
- Ciclohexanocarbonitrilo
- 2-Metilpentanonitrilo
- Etanodinitrilo (cianógeno)
- Propanodinitrilo